Comment fabriquer une colle naturelle ?
L'Homme est capable de produire des colles chimiques, comme celles que l'on trouve dans beaucoup de tubes vendus dans le commerce.
Mais il est également possible de produire des colles totalement naturelles à base de matière animale et végétale, c'est-à-dire sans produits chimiques de synthèse dangereux. Tel est le cas des
colles de poissons, d'os, de peau de lapin, d'amidon ...
Ici, nous étudierons la fabrication d'une colle naturelle à base de caséine. Cette colle, réalisable à la maison, est considérée comme naturelle car elle est synthétisée à partir de produits naturels : le lait et le vinaigre et même si on utilise de l'hydrogénocarbonate de sodium qui n'est pas dangereux.
La colle à base de caséine

En 1897, le chimiste allemand Spittler a découvert la colle de caséine. Elle fut massivement utilisée au début du XXème siècle dans l'industrie aéronautique. En effet, les avions de la première
guerre mondiale ont été assembler avec la colle de caséine.
Qu'est-ce que la caséine ?
La caséine est la principale protéine du lait (3,2 % du lait).
Le lait un mélange complexe constitué d'eau à 87% d'eau, et de nutriments constitués par des lipides, des protéines, des glucides ... . Les caséines sont des macro-molécules (composées de 209 acides aminés) composées d'une longue chaîne carbonée et azotée qui est lipophile* d'un bout de la chaîne et hydrophile* de l'autre. On dit que cette molécule est amphiphile, c'est un tensioactif*.
Pourquoi la caséine précipite t-elle après ajout d'acide ?
Lorsque le pH du lait est compris entre ses valeurs habituelles soit entre 6,3 et 6,6, les protéines sont dispersées dans le liquide et forment une solution homogène. Mais si la valeur du pH diminue par ajout d’un acide, les macromolécules de protéines se regroupent et se lient entre elles pour former un solide insoluble, les micelles de caséines, qui précipite au fond du récipient, ceci lorsque la valeur du pH du lait atteint 4,6. Ainsi, la charge électrique de la caséine varie avec le pH.
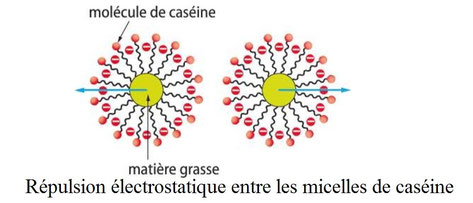
Dans le lait frais, les lipides (insolubles dans l’eau) s’entourent de molécules de caséine, car leur partie lipophile baigne dans la matière grasse et la partie hydrophile reste dans l’eau. Il se forme donc des micelles, qui sont constituées de gouttelettes de matière grasse entourées de molécules de caséine. Le lait est une émulsion*.
Comme la couche externe des micelles est négative, ces dernières se repoussent entre elles, ce qui empêche la précipitation des matières grasses. Mais en faisant varier le pH du lait, on diminue la répulsion électrostatique entre les micelles, cela provoque donc leur précipitation sous forme de grumeaux de matière grasse et de caséine : le caillé. Pour obtenir un bon caillé, il faut chauffer le lait modérément (de 40 à 50°C) et faire varier lentement le pH.
Donc, une micelle de caséine est composée d'une matière grasse au centre, et de molécules de caséine autour.
Pourquoi ajoute t-on de l'hydrogénocarbonate de sodium ?
Ajouter de l'hydrogénocarbonate de sodium permet de retirer l'acide encore présent dans le filtrat. En effet l'hydrogénocarbonate de sodium est une molécule qui neutralise l'acidité, c'est la raison pour laquelle il est bon d'en prendre un peu pour éliminer les brûlures d’estomac ou les remontées acides car
il neutralise l’acide chlorhydrique de l'estomac en le transformant en chlorure de sodium (du sel) et en dioxyde de carbone.
La réaction entre l'acide éthanoïque (noté AH) et l'hydrogénocarbonate de sodium s'écrit :
NaHCO3 + AH ![]() CO2(g) + H2O + NaA(aq)
CO2(g) + H2O + NaA(aq)
Comment colle-t-elle ?
La colle de caséine est une colle colloïdale naturelle car elle est à base d'un polymère naturel, la protéine caséine. Cette protéine est capable de créer des liaisons avec des molécules d'eau comme la Super Glue (beaucoup plus forte bien-sûr).
Réalisation de la colle
Matériel : une casserole, une plaque
chauffante, un agitateur, un pH-mètre, un thermomètre, un dispositif de filtration, une balance et une capsule de pesée.
Produits : Lait, du sodium hydrogénocarbonate, de l'acide éthanoïque
Protocole expérimental :
-
Prélever environ 200 mL de lait, le verser dans une casserole et placer le tout sur une
plaque chauffante.
-
Chauffer tout en remuant jusqu’à atteindre 40°C.
-
Retirer la casserole de la plaque et ajouter goutte à goutte de l'acide
éthanoïque CH3COOH (= vinaigre) jusqu'à obtenir un pH de 4,6 ; l'acide fait précipiter les
molécules de caséine.
-
Filtrer et récupérer la phase solide qui contient la caséine.
-
Ajouter 6g de sodium hydrogénocarbonate NaHCO3 (= bicarbonate de soude). La colle est prête !
Conseil : Ajouter un peu d'acétone pour conserver la colle plus longtemps, car les graisses sont très solubles dans l’acétone contrairement à la caséine donc l’ajout d’acétone permet de séparer la caséine des graisses. Et à conserver hermétiquement fermée au réfrigérateur de préférence.
Ci-dessous, la vidéo de la synthèse de notre colle, si la vidéo ne fonctionne pas, vous pouvez également la visionner ici.
Schéma-bilan
La colle à base d'amidon
La colle à base d'amidon a fait l'objet de notre soutenance oral. Retrouver le Prezi que nous avons réalisé ci-dessous sur la colle d'amidon.

Site de TPE sur les colles - 1ère S - 2014/2015
TAVERNIER Nicolas
BOISSIER Sébastien
Lycée Gaston BACHELARD - 10200 Bar-sur-Aube